Définir molalité.
Molalité (concentration molale):
nombre de moles de soluté par masse de solvant, càd par kg de solvant (mole/kg)
Définir Molarité.
Molarité (concentration molaire):
nombre de moles de soluté par volume de solution, càd par litre de solution (mol/L)
Définir osmolarité:
Osmolarité:
Nombre de particules individuelles par litre de solution (osm/L)
Définir osmolalité:
Osmolalité:
Nombre de particules individuelles de soluté par kg de solvant. (osm/kg)
Indiquer dans quelles conditions molarité et molalité sont équivalentes. Expliquer brièvement votre réponse
Lorsque le solvant est l’eau (1L d’eau = 1kg d’eau)
Si la solution est très diluée (solution idéale), alors la molarité et la molalité sont égales. Poids et volumes des solutés négligeables, donc 1 L de solution = 1 L d’eau = 1kg d’eau.
Molarité = Molalité
Indiquer dans quelles conditions molarité et osmolarité sont équivalentes. Expliquer brièvement votre réponse
Lorsque le soluté est un non électrolyte qui ne se dissocie pas en solution (n=1), alors osmolarité = molarité
osmolarité=molarité [n.y+(1-y)]
n.y est le nombre de particules dissociées
(1-y) est le nombre de particules non dissociées
Indiquer dans quelles conditions molalité et osmolalité sont équivalentes. Expliquer brièvement votre réponse
Lorsque le soluté est un non électrolyte, il ne se dissocie pas en solution
(n=1). L’osmolarité= molarité.
** osmolarité=molarité [n.y+(1-y)]**
**osmolalité. ρ = osmolarité **
**osmolalité. ρ = molalité.[n.y+(1-y)]. ρ **
En conclusion, si le soluté n’est pas un électrolyte alors l’osmolalité=molalité.
Indiquer dans quelles conditions osmolarité et osmolalité sont équivalentes. Expliquer brièvement votre réponse
Lorsque le solvant est l’eau (1L d’eau = 1kg d’eau),
si une solution est très dilutée (solution idéale), alors osmolarité = osmolalité.
Poids et volume des solutés sont négligeables, donc 1L de solution = 1L d’H2O soit 1kg d’eau.
Indiquer dans quelles conditions molarité et molalité sont différentes. Expliquer brièvement votre réponse
Lorsque le solvant est l’eau (1L d’eau = 1kg d’eau)
si la solution n’est pas diluée, alors molalité > molarité.
Le poids et le volume des solutés ne sont plus négligeables, donc 1 L de solution contient un volume moindre d’H2O et donc moins d’1 kg d’eau.
La molarité ne tient pas compte du volume des solutés.
Indiquer dans quelles conditions molarité et osmolarité sont différentes. Expliquer brièvement votre réponse
Lorsque le soluté est un électrolyte qui se dissocie en solution, le nombre de particules (n) résultant de la dissociation est >1.
osmolarité n’est pas équivalente à molarité
osmolarité=molarité [n.y+(1-y)]
n.y est le nombre de particules dissociées
(1-y) est le nombre de particules non dissociées
Indiquer dans quelles conditions molalité et osmolalité sont différentes. Expliquer brièvement votre réponse
Lorsque le soluté est un électrolyte qui se dissocie en solution, le nombre de particules (n) résultant de la dissociation est >1.
osmolarité= molarité. [n.y+(1-y)]
Lorsque le solvant est l’eau (1L d’eau= 1kg d’eau), si la solution n’est pas diluée alors osmolalité> osmolarité, et la molalité>molarité.
De ce fait osmolalité et molalité seront différentes.
Indiquer dans quelles conditions osmolarité et osmolalité sont différentes. Expliquer brièvement votre réponse
Lorsque le solvant est l’eau (1L d’eau=1kg d’eau),
si la solution n’est pas diluée, alors osmolalité > osmolarité.
Poids et volumes des solutés ne sont alors plus négligeables, 1L de solution contient un volume d’H2O moindre, et donc moins d’1kg d’H2O.
Dans le cas du plasma, on utilise régulièrement l’osmolarité et l’osmolalité de façon interchangeable. Expliquer pourquoi il n’est cependant pas souhaitable de procéder de la sorte.
Les liquides corporels ne sont pas des solutions idéales et au niveau du plasma environ 7% du volume est occupé principalement par des protéines, donc l’osmolarité est différente de l’osmolalité.
Cependant osmolarité et osmolalité sont souvent utilisées de façon interchangeable en considérant, par approximation les liquides biologiques comme des solutions aqueuses diluées.
Pour le plasma il est préférable d’utiliser l’osmolalité (non influencée par le volume des solutés).
L’osmolalité du plasma est mesurée par abaissement cryoscopique est ~290 mosm/kg H2O
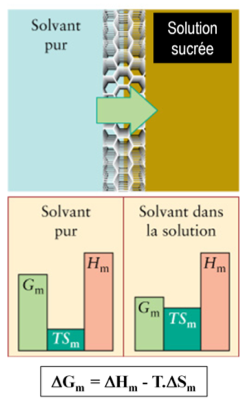
Expliquer le phénomène d’osmose.
L’osmose est le déplacement spontané d’un volume d’eau à travers une membrane semi-perméable, d’un compartiment où l’eau est la plus concentrée vers le compartiment où elle est la moins concentrée.
C’est un processus spontané qui se produit naturellement, sans intervention extérieure, càd sans apport d’énergie extérieure et qui conduit irréversiblement à un état d’équilibre où elle s’arrête.
Ainsi l’osmose est la diffusion de l’eau sous l’effet de son propre gradient qui entraine le déplacement d’un volume de la solution.
Définir la pression osmotique.
La pression osmotique π correspond à la pression hydrostatique qui s’oppose au mouvement d’eau provenant du compartiment le moins concentré en soluté non perméant vers le compartiment le plus concentré en soluté non perméant.
La pression osmotique exercée par une solution est fonction du nombre de particules libres en solution qu’elle contient, indépendamment de leur taille, de leur masse ou de leur valence.
Elle est exprimée par la relation de Van’t Hoff en mmHg (ou atm).
Expliquer brièvement comment la pression osmotique peut être mesurée.
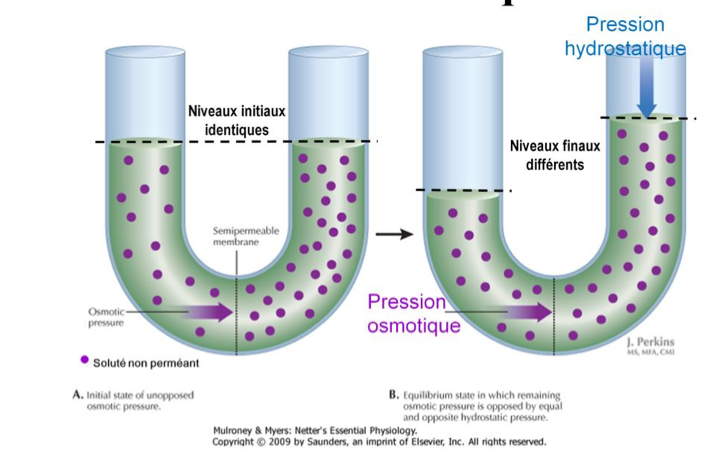
Deux méthodes permettent de mesurer la pression osmotique:
- tube en U:
Un tube en U contenant une membrane semi perméable qui sépare deux compartiments contenant chacun deux solutions de concentrations différentes en soluté non perméant.
L’eau va se déplacer du compartiment le moins concentré vers le compartiment le plus concentré en soluté non perméant.
La pression osmotique est donc la pression hydrostatique qui s’oppose à ce mouvement.
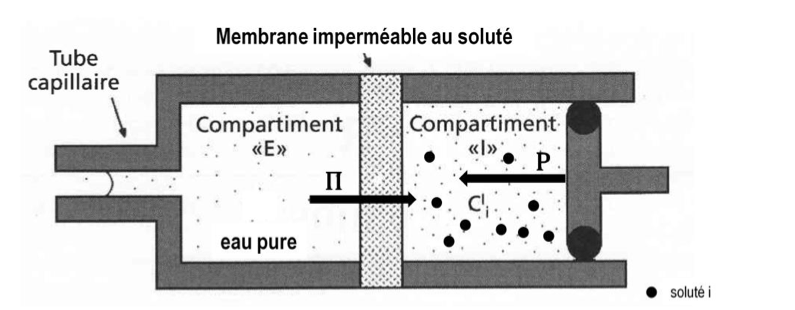
- Modèle du piston et de la membrane semi-perméable
Un compartiment E contient de l’eau pure et est ouvert vers l’atmosphère tandis que le compartiment I est fermé par un piston mobile et contient un soluté i non perméant.
L’osmose entraine un déplacement de volume d’eau du compartiment E dont le volume diminue vers le compartiment I dont le volume augmente et déplace le piston.
La pression qui doit être appliquée sur le piston afin d’empêcher le flux volumique est la pression osmotique.
Indiquer la formule permettant de calculer la pression osmotique.
Relation de Van’t Hoff détermine la pression osmotique (π)
π=i.R.T.C
- π en mmHg (ou atm)
- C: concentration molale (mole/kg H2O)
- i: coeff de Van’t Hoff, indique la proportion de particules libres:
- i= n.y+(1-y)
- soit i= 1 pour non électrolytes, et >1 pour électrolytes se dissociant
- y: le coeff d’activité
- y=1 pour solution idéales très diluées
- y<1 pour solutions non idéales
- n: le nombre de particules résultant de la dissociation
- R constante des gaz parfaits 0,0821 dm3.atm.K-1.mole-1
- T température, en K
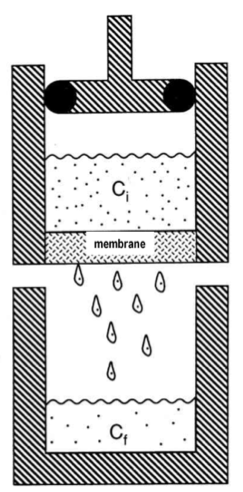
Définir le coefficient de réflexion et expliquer brièvement comment il peut être déterminé pour un soluté et une membrane donnée.
Le coefficient de reflexion de Staverman définit la perméabilité d’une membrane considérée vis à vis d’un soluté donné.
σi= 1 - (Cf/Ci)
- σi: coefficient de réflexion du soluté i pour une membrane donnée, sans dimension.
- Ci: concentration du soluté i dans le compartiment sup (en M)
- Cf: concentration du soluté i dans le filtrat (en M)
3 cas se présentent selon la perméabilité de la membrane à i:
- la membrane est non limitante
(càd totalement perméable à i, il s’agit d’Ultrafiltration)
Ci = Cf => σ = 0 - la membrane est totalement imperméable à i:
Cf = 0 => σ = 1 - la membrane est partiellement imperméable à i:
Cf < Ci et Cf > 0
NB: Cf/Ci = 1 - σ représente le coefficient de tamisage
Définir la pression osmotique efficace et indiquer la formule qui la relie à la pression osmotique théorique.
La pression osmotique efficace (πeff) qui est mesurée, se situe entre 0 et la valeur prédite par la relation de Van’t Hoff (πthéorique).
πeff = σ.i.R.T.C
σi= πeff / πthéo
πthéo = i.R.T.C
σ dont la valeur se situe entre 0 et 1 permet de tenir compte de la semi-perméabilité des membranes pour les solutés considérés et de déterminer la pression osmotique efficace exercée par la solution.
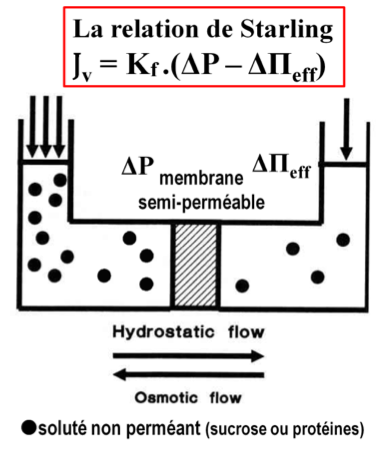
Indiquer la forme générale de la relation de Starling. Expliquer comment cette relation est établie entre les deux compartiments séparés par une membrane semi-perméable.
Lorsque la pression hydrostatique et la pression osmotique agissent simultanément au niveau de la membrane
Jv= (Lp.A.ΔP) - (Lp.A.Δπeff)
Jv= Lp.A.(ΔP - Δπeff)
Jv=Kf.(ΔP-Δπeff)
Jv=Kf.(ΔP-σ.Δπth)
est la relation de Starling qui guide les échanges liquidiens au niveau de la paroi des capillaires.
Lorsque les pressions hydrostatique et osmotique se compensent exactement:
Δπeff = ΔP et Jv=0
- Jv: le flux d’eau (mL/sec) ou (cm3/sec)
- ΔP: différence de pression hydrostatique au niveau de la membrane (atm)
- Δπth: différence de pression osm théorique (Van’t Hoff) au niveau de la membrane (atm)
- Kf: coefficient de filtration en (cm3/sec.atm)
- σ: coefficient de reflexion de la membrane
NB: au niveau d’une membrane cellulaire, la ddp° hydrostatique est nulle. Le flux d’eau (Jv) est exclusivement conditionné par la ddp° osmotique.
Jv=Kf.Δπeff
Définir l’effet solvant et donner la formule générale qui permet de le calculer.
L’effet solvant est l’entrainement du soluté à travers une membrane par le flux volumique: un flux d’eau à travers une membrane entraine également un passage de petites molécules en fonction de leur coefficient de reflexion (σ<1)
L’effet solvant ou flux convectif du soluté i (Ji)
Ji=Jv.(1-σ).Ci
- si σi=0 il s’agit d’ultrafiltration pure donc Cf=Ci et Ji=Jv.Ci
- si σi=1 alors Cf=0 et Ji=0
NB:
le flux du soluté i = flux diffusif de i + flux convectif de i et est donné par la relation: Ji=Pi.ΔCi +Jv.(1-σ).Ci
avec Pi le coeff de perméabilité de la membrane (cm.sec-1 )
Définir la tonicité.
La tonicité est l’osmolalité effective, càd la concentration des osmoles effectifs.
- un osmole effectif est non perméant et exerce une pression osmotique
- un osmole non effectif est perméant et ne peut exercer une pression osmotique.
Le nombre d’osmoles effectifs d’un compartiment détermine les mouvements d’eau au niveau de ce compartiment et conditionne son volume.
Tonicité = (osmolalité) - (osmolalité non effective)
<u>NB: </u>par convention la tonicité d’une solution se définit par rapport au volume de la cellule qui est placée dans cette solution.
Soit une cellule fictive plongée en solution expliquer pourquoi l’addition au MEC d’un soluté non perméant induit une variation durable du volume cellulaire.
Soit deux compartiments aqueux de volume égal séparés par une membrane semi-perméable (imperméable au soluté i qui ne se dissocie pas, et perméable à l’eau).
état initial:
- V1=V2=1L
- Le soluté i est plus concentré dans le compartiment 2:
- C2i= 4 osm > C1i= 2osm
- L’eau est plus concentrée dans le compartiment 1:
- C1H2O = 53,5 M et C2H2O = 51,5 M
- le flux net d’eau est dirigé de 1 vers 2.
à l’équilibre
- Mêmes concentrations du soluté i et d’eau dans les deux compartiments qui ont changé de volume.
- V1= 0,67 L et V2= 1,33L
- C1i=C2i= 3M (3osm) et C1H2O = C2H2O = 52,5M
- (La membrane se déplace)

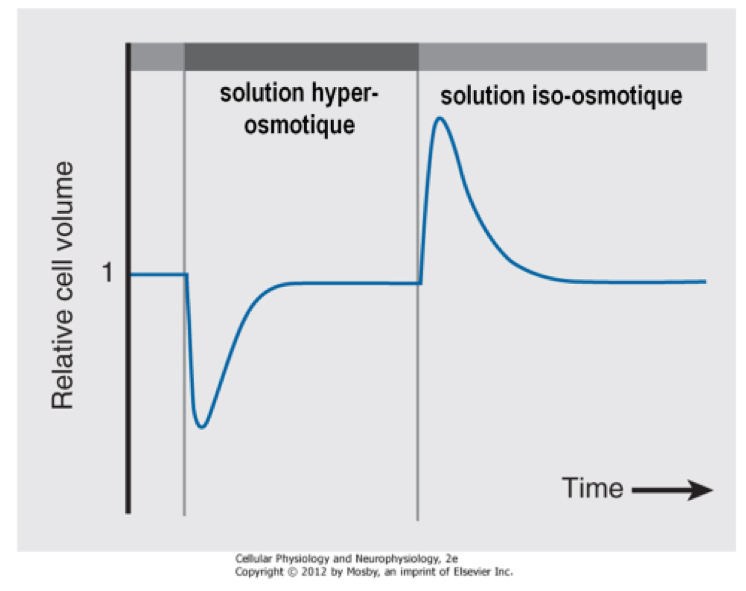
Soit une cellule fictive plongée en solution expliquer pourquoi l’addition au MEC d’un soluté perméant induit une variation transitoire du volume cellulaire.
Cellule hypothétique, initialement placée dans un milieu iso-osmotique et isotonique.
A. remplacement du milieu extracellulaire par un milieu hyperosmotique contenant un soluté perméant:
- La cellule diminue rapidement d evolume suite au passage très rapide d’eau.
- La cellule récupère ensuite progressivement son volume initial: le soluté perméant diffuse selon le gradient de concentration vers l’intérieur de la cellule, augmente progressivement l’osmolarité cellulaire et entraine une entrée d’eau.
- À l’équilibre, la concentration du soluté perméant est identique de part et d’autres de la membrane cellulaire, il n’y a plus d emouvement net du soluté perméant et le volume cellulaire qui est revenu à son état initial, ne varie plus.
- in fine, le soluté perméant n’a pas entrainé de variation de volume.
B. replacement de la cellule qui a été plongée dans le milieu hyperosmotique dans le milieu iso-osmotique et isotonique initial:
- la cellule qui contient le soluté perméant est hyper-osmotique et augmente rapidement de volume suite au passage très rapide d’eau.
- la cellle recupère ensuite progressivement son volume initial: le soluté perméant diffuse selon le gradient de concentration vers l’extérieur de la cellule, diminue progressivement l’osmolarité cellulaire et entraine une sortie d’eau.
- à l’equilibre, la concentration du soluté perméant est identique de part et d’autre de la membrane cellulaire, il n’y a plus de mouvement net du soluté permant et le volume cellulaire qui est revenu à son état initial ne varie plus.
- in fine, le soluté perméant n’a pas entrainé de variation de volume.