Vad står CRISPR/CAS9 för?
Clustered Regularly Interspaced Short Palindromic Repeats/ CRISPR associated system number 9.
Vad är CRISPR/CAS9?
- Ett molekylärbiologiskt system som har justerats för att kunna användas som metod för genmodifiering.
- CRISPR är en DNA sekvens bestående av återkommande korta palindromiska segment (segment som kan läsas på samma sätt åt båda håll).
- Mellan de upprepade segmenten finns så kallade spacers, vilket är korta varierande sekvenser av samma längd.
- Cas9 är ett endonukleas som kan klyva dsDNA.
- Systemet kommer ursprungligen från bakterier, där det fungerar som ett adaptivt immunförsvar, vilket kommer förklaras mer i detalj senare under presentationen.
Beskriv förloppet från upptäckt till metod
- 1987 beskrevs CRISPR sekvensen hos E.coli för första gången (man visste dock inte ännu dess funktion). Upptäckten gjordes av en slump av en forskargrupp på Osaka University ledd av Yoshizumi Ishino då man råkade klona en del av en CRISPR sekvens när man ville studera genen för alkaliskt fosfatas hos bakterien.
- 2002 upptäcktes konserverade gener som associerades med CRISPR regioner i DNA av forskaren Ruud Jansen vid Utrecht University. Dessa visade sig koda för olika helikaser och endonukleaser och benämndes som Cas (crisper associated system).
- 2005 CRISPRs funktion upptäcktes. Forskaren Francisco Mojica upptäckte att spacer sekvenser mellan de återkommande segmenten matchade med gensekvenser hos bakteriofager och plasmider.
- 2009 upptäcktes hur Streptococcus pyogenes utnyttjade enzymet CAS9 i sitt försvar mot virusangrepp av en forskargrupp i ledning av Emmanuelle Charpentier vid Umeå Universitet.
- 2012 Lyckades forskarna Emanuelle Charpentier och Jennifer Doudna framställa ett stabiliserat Cas9 som kan användas för manipulering av specifika DNA sekvenser.
- Sedan Emanuelle Charpentier och Jennifer Doudnas upptäckt 2012 har metoden utvecklats vidare av flera olika forskare och applicerats inom många olika områden. Finns i dagsläget flera tusentals publicerade studier där metoden använts.
Det finns tre olika metoder att förändra DNA, vilka är de?
- Traditionell genteknik
- där hybridnukleinsyra eller rekombinant-DNA bildas.
- En bit DNA sätts in i arvsmassan.
- En mutant eller GMO bildas.
- Konventionella mutationstekniker där slumpmässiga mutationer uppstår.
- Nya tekniker som kan skapa riktade mutationer.
Sedan 1930-talet har man inom växtförädlingen använt strålning eller mutationsframkallande ämnen för att öka den genetiska variationen och på så vis få växter med nya egenskaper.
Till skillnad från genomredigering, där man på förhand kan bestämma var i arvsmassan mutationen ska hamna, är den traditionella mutationsförädlingen slumpmässig och förädlaren får i efterhand analysera om någon av alla de mutationer som uppstått lett till en för människan viktig egenskap.
Zinkfingernukleas-tekniken och meganukleas-tekniker började utvecklas redan under 1990-talet och under 2009 började även TALEN-tekniken användas. Gemensamt för dessa tekniker är att:
- nukleaset kombineras ihop med proteiner som känner igen en viss sekvens av DNA.
- När nukleaset klipper isär DNA-strängen reagerar organismens eget reparationssystem och skadan lagas.
- När DNA-sekvensen lagats och förändringen är klar har det skapats en mutation.
*Under 2013 fick CRISPR/Cas9-tekniken sitt stora genomslag.
Jämföresle av CRISPR/CAS+ och ZFN och TALEN
Om man ska jämföra ZFN och TALEN med CRISP: så är det CRISPR som fått det största genomslaget inom gentekniken
Kan bero på att detta är en mycket enklare och mer anpassningsbar teknik, den är även betydligt billigare och snabbare.
Man får även bättre resultat än med de andra metoderna även om det fortfarande finns utmaningar.
Till skillnad från CRISPR kräver ZFN och TALEN att man inför varje ny målsekvens måste tillverka nya nukleaspar vilket är mycket tidskrävande.
hur fungerar CRISPR/CAS9 i bakterien?
I bakterien är CRISPR/CAS ett adaptivt immunförsvar. CRISPR är ett lokus i bakteriens genom och cas är proteiner som har olika funktioner i det adaptiva immunförsvaret. CRISPR/cas systemet sparar gensekvenser från invaderande virus för att sedan använda dessa som ett immunologiskt minne som sitter i det egna genomet.
Primär infektion
Bakteriofagern injicerar sin arvsmassa i den bakteriella cellen -> för att utnyttja bakteriens enzymer för sin replikation.
Då kommer det virala DNAt att lagras i ett som tidigare nämt CRISPR locus.
Vad är ett CRISPR LOCUS?
CRISPR lokus innehåller en eller flera sekvenser som är komplementära till sekvenser från virusets DNA. De insatta virus-sekvenserna kallas för ”spacers.
CAS eller då cas9 står för själva immuniteten, då det är det som klyver virus DNA:t och gör det oanvändbart. För att detta skall fungera behövs komponenterna tracrRNA och crRNA. crRNA fås när CRISPR lokuset transkriberas och har som uppgift att guida cas9 till rätt spacer.
Det hela fungerar genom att crRNAt kommer baspara med tracerRNA och crRNAt kommer då associera med Cas9.
CAS9 känner ej igen ett specifikt klyvningsite utan det är istället en PAM sekvens som avgör var i en en spacer cas9 skall klyva. PAM är en mycket konserverad sekvens.
Sekundär infektion
Vid en sekundär infektion så kommer crRNAt att baspara med den komplementära sekvensen i det virala DNAt vilket medför att Cas proteinet kommer klyva DNAt.
Skiljer sig från humant
Denna typ av adaptivt immunförsvar skiljer sig från de humana då en inkorpering sker i genomet och kommer att replikeras vid celldelning.
Detta medför så ledes att immunitet förs vidare vertikalt och att alla dotterceller kommer ärva denna immunitet.
Hur tar vi kunskapen från bakterien till labbet?
- Nu vet vi hur systemet i bakterien fungerar så nu kan vi utnyttja bakteriens system i labb.
- Vi vet hur Cas proteinerna är uppbyggda så kan vi återskapa de själva, men vi kan också rena fram de ur bakterier.
- Sen kan vi designa ett guideRNA (tracerRNA + crRNA) som binder till Cas och en “spacer” som är komplementärt till den gen vi är intresserade av att klyva.
- Vi introducerar sedan detta i cellen via transfektion
- Efter dubbelsträngsbrott behöver cellen laga skadan och vår önskan är att den gör det via homolog rekombination.
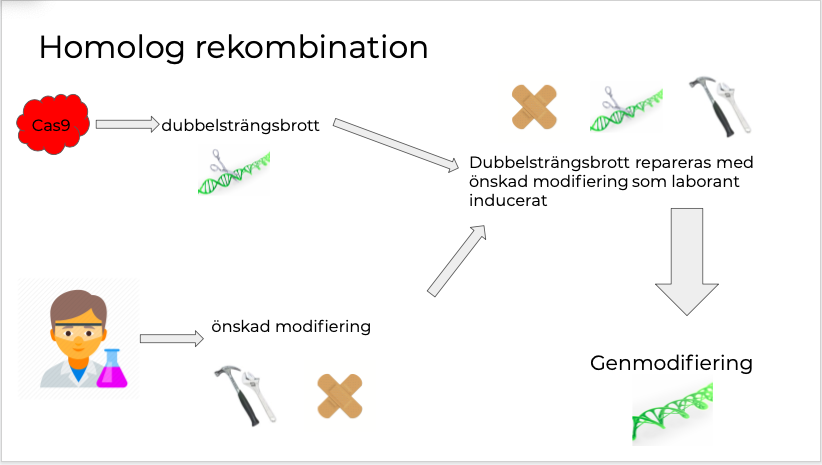
Beskriv homolog rekombination
Homolog rekombination
- Cas9 kommer orsaka ett DNA-dubbelsträngsbrott på specifik plats i genomet.
- Som laborant introducerar du en homolog reparationsmall som innehåller önskad genommodifiering.
- Dubbelsträngsbrottet repareras genom homolog rekombination med den önskade genmodifieringen som du som laborant inducerat.
- På detta sätt kan du som laborant generera raderingar och punktmutanter med mera.
Homolog rekombination är en snabb och billig metod men för att komma dit behöver ett förarbete göras.
- Önskad genetisk manipulation
Den första frågan du behöver ställa dig i planeringen av ditt CRISPR-experiment är, vill du:
- Generera fullständig och permanent förlust av genuttryck eller funktion ( knockout )?
- Generera en specifik mutant allel av en gen ( punktmutant )?
- Öka eller minska uttrycket av en målgen?
När du vet vad du vill vill göra och har ditt mål klart kan planeringen av experimentet starta.
Konstruerade CRISPR-system innehåller två komponenter:
- guide-RNA (gRNA)
- Cas-protein
- Val av Expression System
Maskineriet bestående av gRNA och CAS måste finnas uttryckt i målcellerna, detta möjliggörs via transfektion. ( hur ska transfektion göras?)
- Val av Målsekvens och utformning av ditt gRNA
Vid val av målsekvens måste man tänka att cas ska kunna binda till PAM som fungerar som en promotor för Cas9. Målsekvens ska också vara unik för den genen så att ej samma sekvens finns på andra gener för då kommer klyvning uppstå där.
Användningsområden?
Hur kan CRISPR/cas9 uttnyttjas i livsmedelsindustri?
Inom livsmedelsindustrin kan man redan nu tänka sig att det finns många fördelar med denna metod.
Genom att modifiera generna hos grödor kan man exempelvis göra att de växer snabbare, eller är mer tåliga mot bekämpningsmedel, eller att de håller sig färska längre genom att minska uttryck av nedbrytningsenzymer hos grödan.
Ett exempel på detta: Med CRISPR/Cas9 kan man generera en “knock out”, vilket betyder att man inaktiverar specifika generna hos till exempel tomater som kan resultera i tomater utan kärnor. Detta ses som positivt inom industrin för t.ex. krossade tomater då man ej längre behöver sortera bort kärnor.
Forskare har även lyckats framställa vissa stammar av vete med en minskad mängd av de epitoper som kroppen reagerar på vid glutenintolerans. Detta är dock inte helt färdigställt ännu, och kan som det ser ut nu inte heller komma ut på marknaden här i Europa på grund av strikta lagar när det gäller GMO-produkter.
Kan CRISPR/Cas9 bota genetiska sjukdomar?
Här finns många försök gjorda på djur, exempelvis har man kunnat få ner antalet infekterade celler hos en råtta med 99% HIV-infekterade celler till 48% bara genom injicering av Cas9 i dess svans. Men mycket av behandling av sjukdomar hos människor via CRISPR/Cas9 ligger ännu i framtiden.
Man har dock väldigt nyligen, förra året, använt sig av CRISPR/Cas9 för att försöka bota en kvinna i USA från sickle-cell anemi.
De man gjorde var att ge henne en cytostatika behandling för att supressa hennes befintliga celler i benmärgen
för att sedan transplantera in celler man tidigare skördat från henne själv och genmodifierat med CRISPR/Cas9.
Trots att man trycker ner hennes immunförsvar med cytostatika menar man att man riskerar mindre reaktion från kroppen då man trots allt använder hennes egna celler.
Här vet man ännu inte resultatet, då det kan dröja lång tid innan man kan bekräftat att detta gjort skillnad i detta fallet.
I kina har man även provat lite behandling vid cancer men de finns inget genomslående där än.
Hur kan CRISPR/CAS9 användas i diagnostik?
CRISPR/Cas9 kan även användas, tack vare sin specificitet, inom diagnostiken.
Det finns exempelvis en metod som kallas Sherlock:
- Metod går ut på att man använder sig av ett speciellt typ av Cas-protein, Cas13A.
- Detta protein riktar istället in sig på RNA istället för DNA.
- När det hittat sin målsekvens och klippt den aktiveras CAS och börjar då att klippa andra närvarande enkelsträngade RNA, ospecifikt.
- Om man då tillsatt en enkelsträngad reportersekvens med flouroforer på vardera sida avges flourescens när denna klipps, vilket alltså blir en direkt detektion om Cas-proteinet aktiverats och klippt målsekvensen till att börja med, och är därför en mycket känslig och kvalitativ metod.
Man har också utvecklat snabbtester med hjälp av strips, vilket är väldigt användbart i länder där Zikavirus eller Denguevirus ses exempelvis. Här mäter man inte flourescens, utan utgår från vart reportrarna fastnar vilket beror på om de är kluvna eller ej.
Om reportern är intakt fastnar de på första detektionslinjen. Om reportern är kluven fastnar de i ett senare skede, vilket gör att det blir ett färgomslag högre upp på stripen. (se bild)
Användning av CRISPR/Cas9 i framtiden?
Bota genetiska sjukdomar
Bota många genetiska sjukdomar med CRISPR/CAS9 ligger nära i tiden
det är möjligt i praktiken men den stora frågan blir etiken, är det etiskt rätt att modifiera genomet hos en människa?
Man vet fortfarande för lite om vilka andra konsekvenser det skulle få för människan när man redigerar genomet, och på så sätt blir människan ett vetenskapligt försöksdjur menar man.
Samtidigt menar de som är positiva till att använda CRISPR/Cas9 för att bota genetiska sjukdomar att det är oetiskt att låta ett barn födas med en dödlig genetisk sjukdom som går att åtgärda med CRISPR/Cas9 redan innan födsel.
*De som är viktigt att ha med sig är att om vi börjar modifiera gener på människor så finns det ingen återvändo det är ingenting som försvinner utan det förs vidare generation efter generation.
Användning av CRISPR/Cas9 för att ”förbättra” människan
I teorin så är det möjligt med hjälp av CRISPR/Cas9 att modifiera en människa innan den är ens född till en ”perfekt människa”.
Människan skulle tex kunna ha:
- perfekt syn
- perfekt hörsel
- perfekt lukt
- ökad metabolism
- lättare att bygga muskler
- ökad intelligens
- immun mot alla genetiska sjukdomar
- kanske till och med långsammare åldrande.
Dessa är saker som skulle intressera många människor om CRISPR/Cas9 blir vanligare vid modifiering av det mänskliga genomet och det skulle förändra hela framtiden för den mänskliga rasen.
Utmaningar med CRISPR/ Cas?
Det första problemet är: hur vi skall genomföra en transfektion av celler med CRISPR/ Cas på ett effektivt sätt.
- Det finns ett flertal metoder.
- Val av metod beror på både typ av celler men också typ av vektor.
- En vanlig vektor är adeno-associerat virus, men de har en begränsad kapacitet.
- Också viktigt att tänka på om det ska vara en övergående transfektion eller en stabil transfektion.
Nästa problem är att: Cas har naturligt en viss ”mis-match” tolerans för att kunna identifiera infekterande DNA med små mutationer, vilket i bakterie modellen endast gör den mer effektiv men blir ett problem för oss när vi ska designa de guidade RNA`t.
- Det kan introducera så kallad off target klyvning. Detta kan också ske om guideRNAt inte är helt unikt, vilket kan vara svårt att åstadkomma med korta sekvenser.
Nästa problem: Det finns två huvudstrategier cellen har för reparation av DNA. Den ena är homolog rekombination och den andra är ”non homologous end joining”.
Icke homolog änd-reparation:
- resulterar ofta i olika stora deletioner på grund av att de fria ändarna av DNA hinner brytas ner före de hinner ligeras ihop igen.
- Det kan också resultera i en frame-shift eller olika okontrollerade insertioner.
- Ofta är målet att utnyttja homolog rekombination för att ersätta den sekvensen som klyvs bort med en annan variant. Det har visat sig vara lättare sagt än gjort då det kräver att den ersättande sekvensen måste vara i närheten när klyvningen sker och det är en mekanism som involverar 21 olika proteiner.
ett annat problem: Det har även upptäckts att användandet av Cas9 i somatiska celler har initierat ett T-cells svar i vissa experiment.
I dagsläget är det fortfarande okänt vad många gener har för funktion Vi har alltså ingen aning om vad som skulle hända om vi gick in och började ändra i flera gener hos humana embryon.
- Det skulle dessutom ta enormt lång tid att få reda på, på grund av vår långa generationstid. Även vid perfekt utförda experiment.



