Fonctions de l’hémoglobine
- Transport de l’O2 des poumons aux tissus.
- Transport du gaz carbonique des tissus aux poumons.
- Maintien du pH sanguin de 7.35 – 7.45
Transport de l’O2
- La plus grande partie de l’O2 dans le sang est combinée à l’hgb.
- L’O2 et l’hgb se lient facilement et de façon réversible. • Hgb + O2 = Oxyhémoglobine
- Hgb non liée à l’O2 = hgb réduite
- L’hgb a une grande affinité pour l’O2 et pour cette raison qu’il est son principal agent de transport.
- L’hgb tend à devenir complètement saturée en O2 (environ 96%), ce qui veut dire que : 1.39 ml d’O2 pour chaque gramme d’hgb.
- Comme on a déjà vu, c’est le fer de l’hgb qui fixe l’O2.
- On a vu aussi que l’hgb comporte 4 atomes de fer, donc chaque molécule d’hgb peut fixer 4 molécules d’O2 et sera donc l’oxyhémoglobine.
Hgb + O2 =
Oxyhémoglobine
Hgb non liée à l’O2 =
hgb réduite
L’hgb tend à devenir complètement saturée en O2 (environ 96%), ce qui veut dire que :
1.39 ml d’O2 pour chaque gramme d’hgb.
On a vu aussi que l’hgb comporte
4 atomes de fer, donc chaque molécule d’hgb peut fixer 4 molécules d’O2 et sera donc l’oxyhémoglobine.
Production du gaz carbonique
- Le transport entre les poumons et les tissus se fait par l’intermédiaire du sang.
- L’O2 (de l’air) est transportée dans le sang sous 2 différentes formes :
- 1.5 % dans le plasma sous forme dissoute
- 98.5 % dans les gr. Sous forme de combinaison chimique par l’hgb
Parce que 98.5 % de l’O2 est liée à l’hgb est emprisonné dans le gr., seulement l’O2 dissous (1.5 %) peut diffuser des capillaires vers les cellules des tissus.
Transport du gaz carbonique
• Il est produit par la respiration cellulaire (dégradation complète du glucose en présence d’O2, permettant une libération totale de son énergie).
C6H12O6 + 6O2 → 6CO2 + ATP et chaleur
Transport du gaz carbonique Il est transporté sous 3 formes :
- À l’état dissous : Environ 5 % est dissous dans le
plasma. Quand il arrive dans les poumons, il diffuse
dans les alvéoles.
2.Sous forme de bicarbonate : Environ 70 %.
CO2 + H2O (de dans le sang) → H2CO3
Le H2CO3 dans les gr. va être catalysé par anhydrase carbonique et va se dissocier en bicarbonate et ion d’hydrogène.
H2CO3 → HCO3 + H+
- Sous forme de carbaminohémoglobine (ou
carbhémoglobine) : Environ 25 % Le CO2 va se lier à
l’hgb désoxygénée.
Hb + CO2 → HbCO2
On a vu que certains facteurs influencent la liaison ou la dissociation de l’o2 à l’hgb.
La PO2 est la plus importante.
La quantité d’O2 qui se lie à l’hgb est d’autant plus grande que la PO2est élevée.
Quand toute l’hgb réduite est convertie en HbO2, on dit que l’hgb est pleinement saturée.
Quand l’hgb forme un mélange de Hb et de HbO2, elle est partiellement saturée.
Le % de saturation de l’hgb exprime la saturation moyenne de l’hgb en oxygène.
exemple: si toutes les molécules d’hb sont
combinées avec 2 molécules d’O2,
l’hb est saturée à 50 % parce que le maximum
est de 4 molécules d’O2.
Quand toute l’hgb réduite est convertie en HbO2
on dit que l’hgb est pleinement saturée.
Quand l’hgb forme un mélange de Hb et de HbO2
elle est partiellement saturée.
Effets du déplacement de la courbe de dissociation de l’oxyhémoglobine
L’affinité de l’hémoglobine pour l’oxygène est généralement définie comme la pression d’oxygène à laquelle l’hémoglobine est saturée à 50 % ou P50

Facteurs influençant la dissociation de l’hémoglobine
Température du corps :
L’augmentation de la température diminue la saturation de l’hgb et déplace la courbe vers la droite. Comment?
Quand la To augmente, la quantité d’O2 libérée par l’hgb augmente aussi.
Les cellules métaboliquement actives ont besoin d’une plus grande quantité d’O2 et libèrent plus d’acide et de chaleur.
L’acide et la chaleur vont favoriser la libération d’O2 de l’oxyhémoglobine.
À l’inverse, quand il y a hypothermie, le métabolisme cellulaire ralentit, le besoin d’O2 diminue et une plus grande quantité d’O2 reste liée à l’hgb.
……Facteurs influençant la dissociation de l’hémoglobine
- pH sanguin
Effet Bohr
Contrôle du pH : pH = HCO3 (reins)
pCO2 (poumons)
Acidité augmente ; pH diminue, affinité de l’hgb pour l’O2 diminue, donc la dissociation augmente.
Ce qui veut dire : l’augmentation de l’acide favorise la libération de l’O2 par l’hgb.
À mesure que l’hgb devient désoxygénée, l’entrée du CO2 dans les gr. est plus facile et se transforme en bicarbonate grâce à l’anhydrase carbonique.
Quand le pH diminue, la courbe se déplace vers la droite.
À l’inverse, l’augmentation du pH augmente l’affinité de l’hgb pour l’O2 et déplace la courbe vers la gauche.
…….Facteurs influençant la dissociation de l’hémoglobine
- Concentration sanguine en CO2 :
Aussi liée à l’effet de Bohr et donc au pH.
La concentration sanguine augmentée en CO2 augmente la libération de l’O2 dans les tissus et dévie la courbe à droite.
La diminution de la concentration en CO2 à l’effet inverse.
…….Facteurs influençant la dissociation de l’hémoglobine
- Concentration en 2,3-DPG :
L’affinité de l’hgb pour l’O2 est en proportion inverse de la quantité de 2,3-DPG dans la molécule d’hgb.
Si le 2,3-DPG augmente, l’affinité diminue et la dissociation augmente, donc la courbe se déplace vers la droite.
Au contraire, si le 2,3-DPG diminue, l’affinité augmente et la dissociation diminue donc la courbe se déplace vers la gauche.
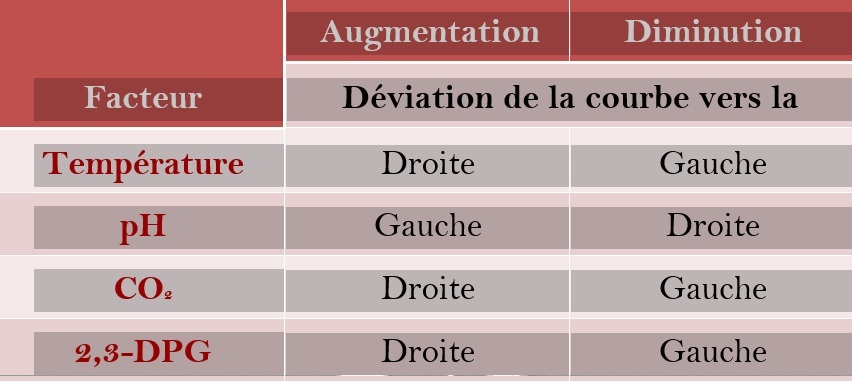
Effets des différents facteurs sur la courbe de dissociation de l’oxyhémoglobine