Wo hängt die Aminogruppe bei Proteinegonen Aminosäuren?
- am α-Kohlenstoff, also α-ständig
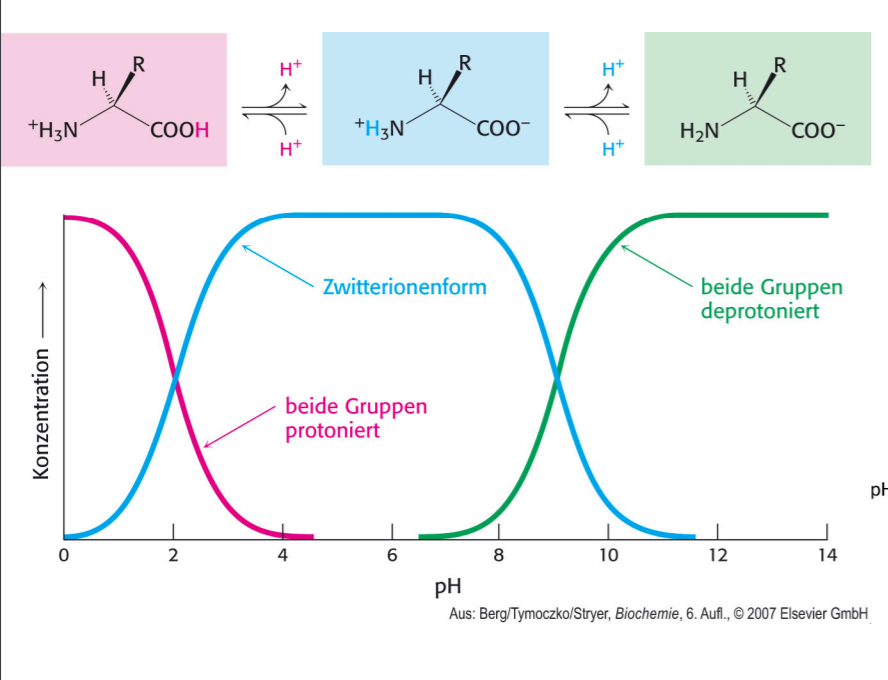
Welche Protonierungszustände haben Aminosäuren und welcher kommt bei physiologischen Bedingungen vor?
- beide protoniert( sehr niedriger pH-Wert) -zwitterionisch(bei pH von ca. 4-8
- > physiologisch relevant
- deprotoniert( bei sehr hohem pH-Wert)
Welche Aminosäure hat keine Enantiomere? Warum?
- Glycin
- alpha-Kohlenstoffatom ist nicht chiral
Was ist eine aliphatische Seitenkette?
-Alkylrest
Was ist die massenreichste Aminosäure?
-Tryptophan-> hat Indolrest
Was ist das besondere an Histidin?
- gehört sowohl zu den Aromaten als auch zu den basischen Aminosäuren
- viele Protonierungszustände( Arginin und Lysin fast immer protoniert)
- Imidazol-Seitengruppe
Was ist das besondere an aromatischen Aminosäuren bezüglich ihrer Absorption?
Wobei spielt das eine Rolle?
- Aromatische Aminosäuren haben Absorptionssektren in UV->Bereich
- bei der UV-Vis-Spektrometrie werden diese Aminosäuren benutzt um Proteine zu quatifizieren
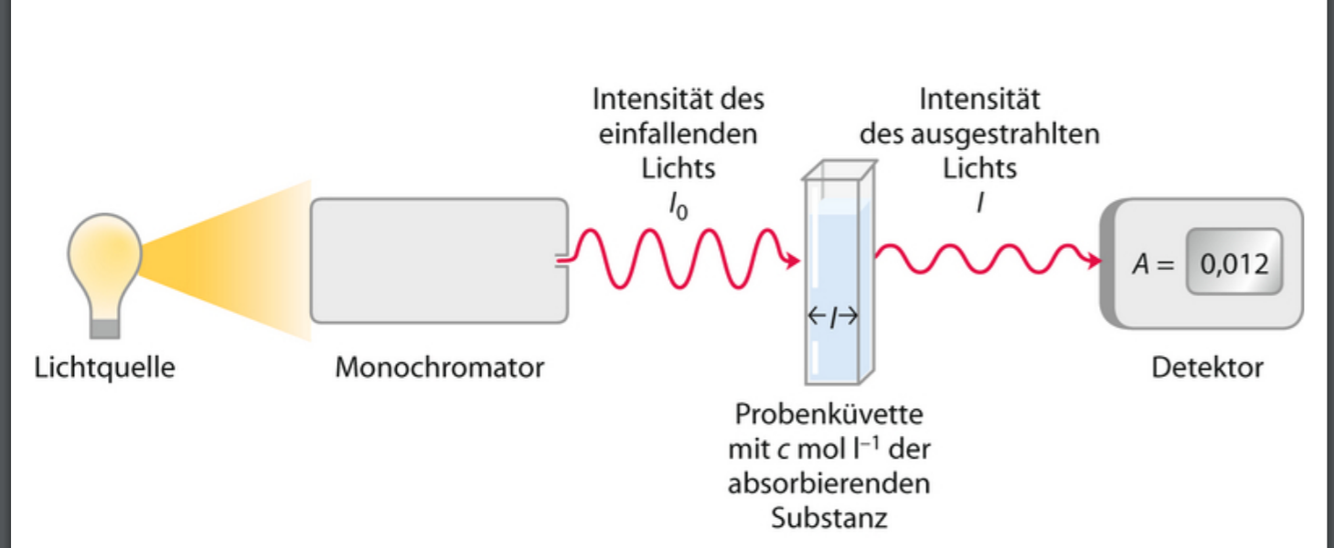
Wie funktioniert die Uv-Vis-Spektrometrie?
Was besagt das Lambert beersche Gesetz?
- Lichtquelle mit polychromatischem licht-> Monochromator->Probenküvette mit mit c mol/ l der zu absorbierenden Substanz und ein Detektor, der Absorption der Substanz misst
- Monochromator fährt durch verschiedene Wellenlängen
E= log l0/l = ε c d
E= Extinktion
ε= Extinktionskoeffizient der Substanz
d= Schichtdicke der Probenküvette
c= Konzentration der Substanz
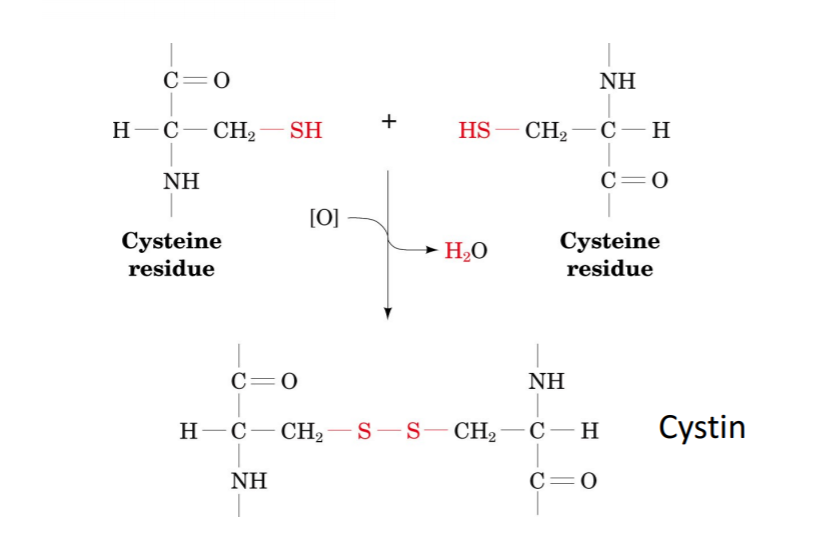
Besonderheiten Cystein
- Thioalkohol
- kann Redoxreaktionen eingehen->d.h. kann oxidieren
- bildet Disulfid, indem Sulfhydrylgruppen oxidieren
- > Insulin
Besonderheit Lysin und Arginin? Was hat es mit der Ladung der Seitenkette des Arginins auf sich?
- positive Ladung-> machen Proteine lösliicher
- hoher Grad an Entropie -> viele Freiheitsgrade durch Rotationsmöglichkeiten der Einfachbindungen
- Arginin: delokalisierte positive Ladung
(Arginin-> längste Aminosäure)
Was bedeutet ein pKa-Wert von 6 für den Protonierungs/-deprotonierungszustand eines Moleküls?
- 1:1 Verhältnis von protonierter und deprotonierter Form bei pH-Wert von 6
Welche Gruppen liegen im physiologischen pH-Wert sowohl protoniert als auch deprotoniert vor?
- Imidazol des Histidins
- die terminale alpha-Aminogruppe( Aminogruppe des N-Terminus)
- Cystein
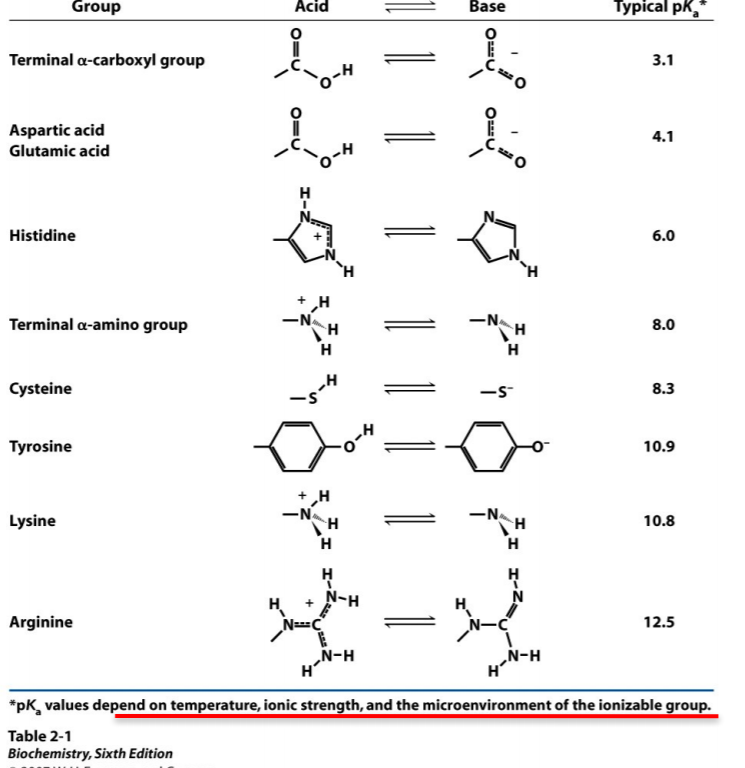
Wovon ist der pKa-Wert ioniesierbarer Gruppen abhängig? Was bedeutet in diesem Zusammenhang Mikroumgebung?
- Temperatur,Ionenstärke und Mikroumgebung
- Mikromumgebung: WW in Umgebung
Was ist die dominante Protonierungsform von Aspariginsäure und Glutaminsäure?
-deprotonierte Variante -> Aspartat und Glutamat
Was hat es mit Aminosäuren mit Carboxamidfunktion in Seitenkette auf sich?
-nie protoniert unter physiologischem pH-Wert
im Gegensatz zur terminalen Aminogruppe des Lysins
-
-Warum gibt es Aminosäuren mit gleichen Verbindungen in 2 Varianten?
-chiraler Kohlenstoff-> Kohlenstoff mit 4 Substituenten -> lässt 2 versch. Möglichkeiten zu Substituente anzugliedern-> Spiegelsymmetrie
L und D AMinosäuren
Isomerie nach Fischer und CIP Regel?
L= S
D=R
Was ist eine Peptidbindung? Was versteht man unter einer Kondensationsreaktion?
- Peptidbindung: Aminogrupe und Carboxylgruppe
- Kondensationsreaktion: 2 Stoffe zu größerem unter Abspaltung von Wasser
Peptide sind polar. Was bedeutet das?
- haben Unterschiedliche Enden
- freie Aminogruppe -> Carboxylatgruppe
Was sind typische Modifikationen von Aminosäuren?
-Methylierung, Acetylierung, Hydroxylierung, Methylierungen, Phosphorylierungen


