Selektivität
Strategien zur Affinitätserhöhung
kein “off-target”
- Shape complementarity
- Shape complementarity with Clash (bsp COX1 und COX2)
- elektrostatische WW, Donor-Akzeptor-Beziehungen
- Allosterie
- Flexibilität des Rezeptors
- explizite Wassermoleküle

Halogen binding
Interaktionen Aromaten mit Halogenatomen
Eigenschaften?
- Halogene findet man in vielen Arzneistoffen
- Allerdings (bislang) kein Teil des rationalen Wirkstoffdesigns
- (Ausnahme: Metabolisierungsschutz (Caro-F, para))
Halogen-Brücke: D-X —- A (D-Donor, A-Akzeptor)
Grund:Elektronenverteilung nicht gleichmäßig (“sigma-whole”)

Halogen binding
Bindungsgeometrie?
Mögliche Akzeptoren?
Bindung X-Akzeptor =3 A° ;Winkel nahe an 180°>(ungefähr gleich wie H-Brücke)
Mögliche halogen-bond Akzeptoren:
• O (Amid) – aus Protein backbone
• OH – aus Ser/Thr/Tyr
• COO- - aus Asp/Glu
• S – aus Cys/Met
• N - aus His
Halogen Bindung
Bindungsenergien der einzelnen Halogenatome?
Ranking?
Was muss ich beim Einbau von Iodmolekülen beachten?
- Cl 1,57 kJ/mol
- Br 3,09 kJ/mol
- I 5,59 kJ/mol
- Vgl. H-bond 2-6 kJ/mol
I > Br > Cl
Beachte Schilddrüsen-WW beim Einbau von Iodmolekülen
Design kovalenter Inhibitoren
Warum kovalent Inhibieren?
- Bindungskinetik: Entkopplung Pharmakokinetik und Pharmakodynamik
- residence-time
a)klassisch nicht kovalente WW b)kovalent reversibel c)kovalent irreversibel
Nur der nicht kovalent gebundene Inhibitor kann verstoffwechselt werden,kovalent gebundener Inhibitor hat seinen Effekt längerfristig
(wenn irreversibel:bis zur Neubildung des Targets)

Design kovalenter Inhibitoren
Herausforderungen?
- zusätzliche Energiebetrachtungen notwendig:
- Assoziation zum nicht- kovalenten Komplex
- Reaktion zum kovalenten Komplex
- müssen für beide Reaktionen das DELTA G abschätzen können
Kovalente Inhibitoren
potenzielle Targets?
- Proteasen
- Kinasen (Rkt mit nicht aktivierten Aminosäuren)
Kovalente Inhibtoren
Reaktionen mit Targets?
- SN
- Michael-Additon
- Addition zu Nitrilen
- Addition zu Aldehyden
- Addition zu Ketonen
- Ringöffnung
- Disulfidbildung
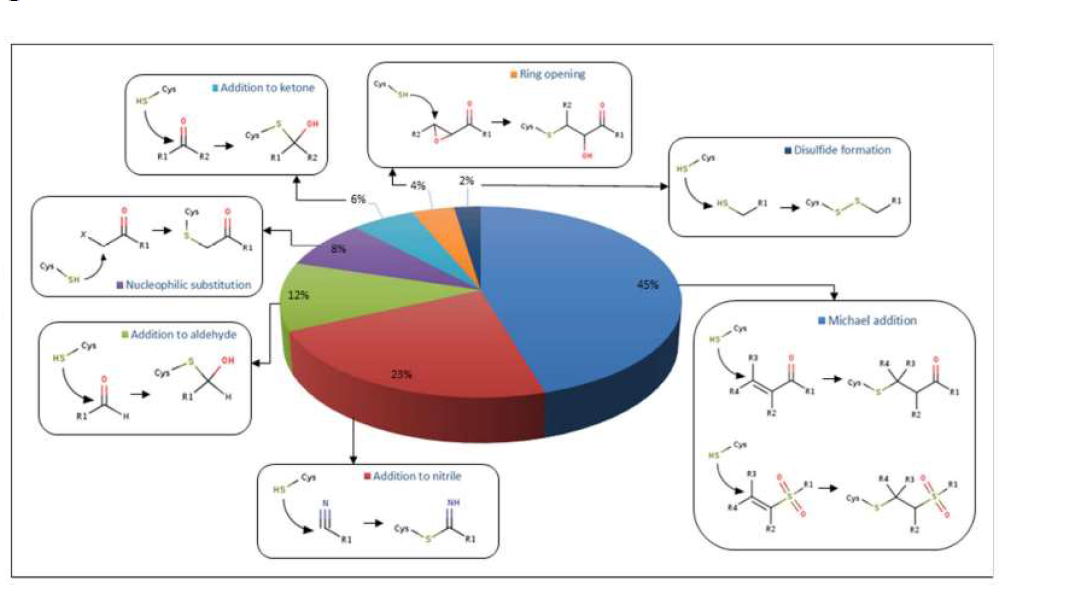
kovalente Inhibitoren
irreversibel oder reversibel?
Vor- und Nachteile
Nachteile irreversibel kovalente Inhibitoren:
- Rkt. mit off-target>ebenfalls vollkommene Inhibition
- ausgeschaltete Targets werden iwann Proteolytisch zersetzt>Addukt zwischen Inhibitor und Spaltprofukt könnte Immunreaktion auslösen
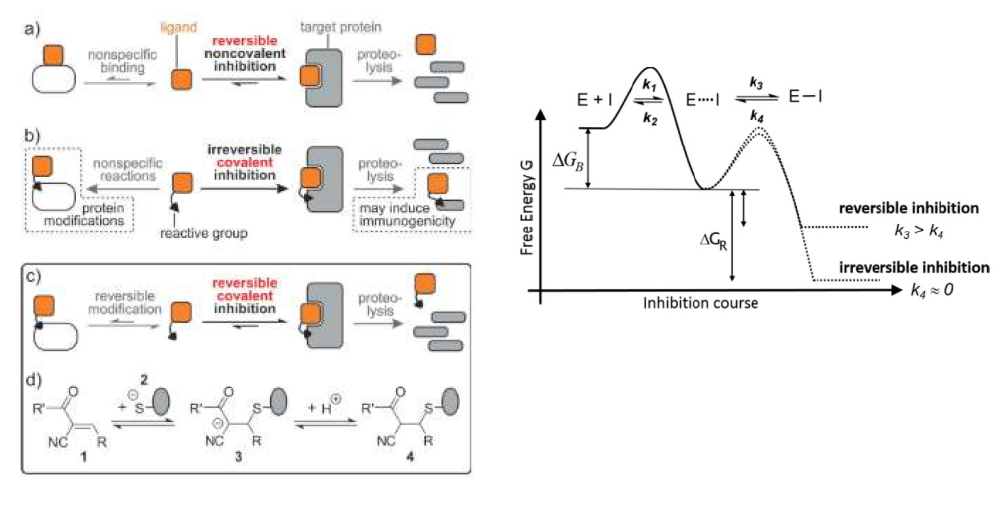
Wie bekomme ich einen irreversiblen kovalenten Inhibitor reversibel?
- am Beispiel Michael-Akzeptor: wenn in alpha-Position elektronenziehende Gruppe wie CN kann Ligand reversibel werden:
- nach katalytischen Angriff des Cysteins >negative Ladung die “umklappen kann”
- CH-Acides C-Atom
- durch sterische Hinderung wie tert-Butylrest Abschirmung des H mgl>>Erhöhung residence time des reversiblen Inhibitors

Protein-Protein-Docking
Wozu?
- Strukturen von Multi-Protein Komplexen (schwer zu kristallisieren)
- Antigen-Antikörper Wechselwirkungen
- Cave:
-Konformationsänderung bei Bindung
-Double modelling (z.B. Homologie-Modell > Komplex)
-viele Freiheitsgrade
Protein-Protein-Docking
Mit welcher Methode am besten Simulierung?
Vorteile?
- Coarse graining Methode :
- United atom beats:AS werden nicht als einzelne Atome dargestellt, sondern als 1 Beads der die Eigenschaften der AS charakterisiert
- explizite Wassermoleküle werden nicht berücksichtigt
- Vorteile:
- Less rotable bonds
- Less interaction partners
- Less impact of slight conformational changes
Protein-Protein-Docking
Herausforderungen?
- Seitenkettenflexiblität
- Rückgrat-Flexiblität
- Challenging Targets
- Wasservermittelte Interaktionen (Wasser wird komplett ignoriert)
Protein-Protein-Docking
Wie komme ich zu einem affinen Liganden?
Was muss ich berücksichtigen?
DOCKING AS KNOWN

Future of CADD
- Machine Learning
- >Drug design „black box“
- LBDD
- Proteinflexibility (MD / induced fit docking)
- „echte“ ΔG-Berechnung
- Ultra-large library virtual screenings (>>100 Millionen Moleküle)
- De-novo docking / virtual synthesis within the binding site


